Transport du dioxygène :
1. Modes de transport du dioxygène
- 2 % sous forme dissoute dans le plasma.
- 98 % sous forme d'oxyhémoglobine (O₂ fixé sur l'hémoglobine).
2. Structure de l’hémoglobine
- Protéine constituée de 4 globines (2 α + 2 β).
- Chaque globine contient un hème avec un atome de fer ferreux (Fe²⁺).
- Une molécule d’O₂ se fixe sur chaque atome de fer → 4 O₂ par hémoglobine.
3. Formation de l’oxyhémoglobine
- Fixation progressive des 4 O₂ (effet de coopération).
- Se déroule dans les capillaires alvéolaires lors de l’hématose.
- Réaction réversible : Hb+4O2↔Hb(O2)4
4. Facteurs influençant la fixation du dioxygène
Facteurs favorisant la libération de l'O₂ (moins d'affinité de l’Hb pour O₂) :
- ↑ pCO₂ (effet Bohr).
- ↓ pH (sang plus acide).
- ↑ Température (ex. activité musculaire).
- ↑ 2,3 DPG (produit par la glycolyse).
Facteurs favorisant la fixation de l'O₂ (plus d'affinité de l’Hb pour O₂) :
→ Courbe de Barcroft :
- Déplacement à droite = libération facilitée de l’O₂ aux tissus.
- Déplacement à gauche = fixation facilitée de l’O₂ aux poumons.
5. Intoxication au monoxyde de carbone (CO)
- L’hémoglobine a une forte affinité pour le CO.
- Formation de carbhémoglobine → empêche le transport de l’O₂.
- Peut entraîner une intoxication mortelle (ex. chauffage défectueux).
Transport du dioxyde de carbone
1. Modes de transport du CO₂
Le CO₂ circule dans le sang sous 3 formes principales :
- 5 à 10 % sous forme dissoute dans le plasma.
- 20 à 25 % fixé aux protéines → carbamino-protéines (ex : hémoglobine).
- 60 à 70 % sous forme d’ion hydrogénocarbonate (HCO₃⁻).
2. Formation des carbamino-protéines
- Le CO₂ se fixe sur les protéines (ex : hémoglobine, asparagine, glutamine).
- Cela libère un proton (H⁺), ce qui diminue le pH (acidification du sang).
- Réaction réversible : CO2+H2N−R↔−O2C−NH−R+H+
3. Formation de l’ion hydrogénocarbonate (HCO₃⁻)
- Dans les globules rouges, le CO₂ se combine à l’eau (H₂O) sous l’action de l’anhydrase carbonique pour former de l’acide carbonique (H₂CO₃) : CO2+H2O↔H2CO
- L’acide carbonique est instable et se dissocie en : H2CO3↔HCO3−+H+
- Cela acidifie le sang (augmentation de H⁺).
4. Effet de la pO₂ sur le transport du CO₂ (Effet Haldane)
- L’hémoglobine peut fixer du CO₂ sous forme de carbaminohémoglobine.
- Quand il y a moins d’O₂ (forme désoxyhémoglobine), l’hémoglobine fixe mieux le CO₂ → Effet Haldane.
- À l’inverse, quand l’hémoglobine est chargée en O₂, elle relâche le CO₂ dans les poumons pour qu'il soit éliminé.
Mécanisme de diffusion des gaz à travers une membrane biologique :
Les gaz respiratoires (O₂ et CO₂) passent entre les alvéoles pulmonaires et le sang grâce à un gradient de pression : ils se déplacent d’un endroit où la pression est élevée vers un endroit où elle est faible.
1️⃣ Diffusion de l’oxygène (O₂) 🌬️
✅ Pression partielle en O₂ élevée dans les alvéoles (air inspiré).
✅ Pression partielle en O₂ faible dans le sang veineux (pauvre en O₂).
👉 L’O₂ diffuse donc des alvéoles vers le sang pour être transporté aux organes.
2️⃣ Diffusion du dioxyde de carbone (CO₂) 💨
✅ Pression partielle en CO₂ élevée dans le sang veineux (car il vient des organes).
✅ Pression partielle en CO₂ faible dans les alvéoles.
👉 Le CO₂ diffuse donc du sang vers les alvéoles pour être expulsé lors de l’expiration.
3️⃣ Facteurs facilitant ces échanges
✔ Grande surface d’échange des alvéoles pulmonaires.
✔ Paroi très fine facilitant la diffusion des gaz.
✔ Écart de pression important pour l’oxygène, favorisant son passage.
✔ Haute diffusibilité du CO₂, qui compense sa faible différence de pression.
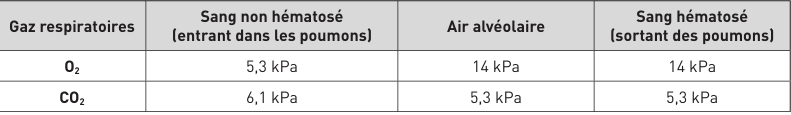
pressions partielles des gaz respiratoires dans divers compartiments du niveau alvéolaire
Échanges gazeux au niveau tissulaire :
Le même principe que précédemment est appliqué. Dans les tissus, les gaz respiratoires diffusent selon leur gradient de pression, le dioxygène diffuse du sang vers les tissus et le dioxyde de carbone, des tissus vers le sang. Dans les tissus, l’équilibre n’est jamais totalement atteint.
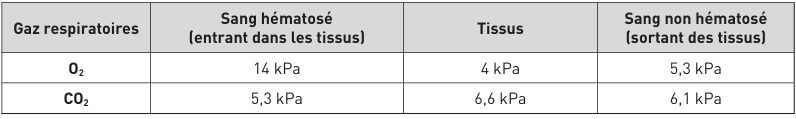
Échanges gazeux au niveau tissulaire



