Terminale
La force des acides et des bases
Définition
- constante d'acidité :
on définit dont le pKA d'un couple acide-base :
pKA = ?log(KA) et ainsi : KA = 10?pKA
- relation entre le pH et le pKa :
- produit ionique de l'eau :
L'eau est une espèce ampholyte. Deux molécules d'eau vont réagir ensemble selon l'équation :
2H2O --> OH- + H3O+
Cette réaction équilibrée s'appelle autoprotolyse de l'eau et est caractérisée par une constante de réaction Ke, appelée produit ionique de l'eau telle que :
soit
à 25°C, Ke = 1,0 x 10-14
on définit le pKe tel que : pKe = -log Ke
à 25°C, pKe = 14
- diagrammes de prédominance et de distribution :
Le diagramme de prédominance d’un couple acide-base AH/A– est un axe gradué en fonction du pH de la solution sur lequel on fait apparaître les domaines de pH dans lesquels l’espèce basique et l’espèce acide prédominent. La valeur frontière de prédominance est le pKA du couple :
• Si pH < pKa :[AH] > [A–]
• Si pH > pKa :[AH] < [A–]
• Si pH = pKa :[AH] = [A–]

Diagramme de prédominance d'un couple acide-base
- diagramme de distribution ?
Le diagramme de distribution d’un couple acide-base AH/A– représente les proportions (en pourcentage) des espèces acide et basique d’un couple en fonction du pH.

Diagramme de distribution d'un couple acide-base
Définition
- force d'un acide ou d'une base :
acide fort / base forte :
acide faible / base faible :
Plus le pKa d'un couple est élevé, plus l'acide est faible et la base forte. Inversement, plus le pKa d'un couple est faible, plus l'acide est fort et la base faible.

Echelle de constante d'acidité et de pKa de certains coules acide-base classique
- composition finale d'une solution acide fort :
Soit une solution de volume invariant V d’acide fort AH de concentration initiale c. La réaction avec l’eau de cet acide étant totale, on obtient à l’état final :
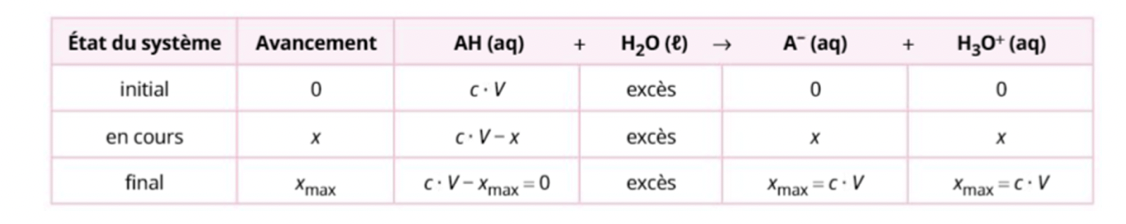
Tableau d'avancement dans le cas d'un acide fort qui réagit totalement avec l'eau
- composition d'une solution d'acide faible :
Soit une solution de volume invariant V d'acide faible AH de concentration initiale c. La réaction avec l'eau de cet acide est équilibrée, on obtient à l'état final :

Tableau d'avancement dans le cas d'un acide faible qui réagit partiellement avec l'eau
Définitions
Terminale
La force des acides et des bases
Définition
- constante d'acidité :
on définit dont le pKA d'un couple acide-base :
pKA = ?log(KA) et ainsi : KA = 10?pKA
- relation entre le pH et le pKa :
- produit ionique de l'eau :
L'eau est une espèce ampholyte. Deux molécules d'eau vont réagir ensemble selon l'équation :
2H2O --> OH- + H3O+
Cette réaction équilibrée s'appelle autoprotolyse de l'eau et est caractérisée par une constante de réaction Ke, appelée produit ionique de l'eau telle que :
soit
à 25°C, Ke = 1,0 x 10-14
on définit le pKe tel que : pKe = -log Ke
à 25°C, pKe = 14
- diagrammes de prédominance et de distribution :
Le diagramme de prédominance d’un couple acide-base AH/A– est un axe gradué en fonction du pH de la solution sur lequel on fait apparaître les domaines de pH dans lesquels l’espèce basique et l’espèce acide prédominent. La valeur frontière de prédominance est le pKA du couple :
• Si pH < pKa :[AH] > [A–]
• Si pH > pKa :[AH] < [A–]
• Si pH = pKa :[AH] = [A–]

Diagramme de prédominance d'un couple acide-base
- diagramme de distribution ?
Le diagramme de distribution d’un couple acide-base AH/A– représente les proportions (en pourcentage) des espèces acide et basique d’un couple en fonction du pH.

Diagramme de distribution d'un couple acide-base
Définition
- force d'un acide ou d'une base :
acide fort / base forte :
acide faible / base faible :
Plus le pKa d'un couple est élevé, plus l'acide est faible et la base forte. Inversement, plus le pKa d'un couple est faible, plus l'acide est fort et la base faible.

Echelle de constante d'acidité et de pKa de certains coules acide-base classique
- composition finale d'une solution acide fort :
Soit une solution de volume invariant V d’acide fort AH de concentration initiale c. La réaction avec l’eau de cet acide étant totale, on obtient à l’état final :

Tableau d'avancement dans le cas d'un acide fort qui réagit totalement avec l'eau
- composition d'une solution d'acide faible :
Soit une solution de volume invariant V d'acide faible AH de concentration initiale c. La réaction avec l'eau de cet acide est équilibrée, on obtient à l'état final :

Tableau d'avancement dans le cas d'un acide faible qui réagit partiellement avec l'eau
