= voie métabolique permettant la synthèse Δ-aminolévulinate - précurseur de la synthèse des porphyrines, à partir du succinate et du glycocolle
-> voie principalement hépatique qui utilise le succinate des mitochondries et le glycocolle
-> synthèse des porphyrines se fait par condensation de 8 molécules de Δ-ALA pour obtenir un noyau tétrapyrole
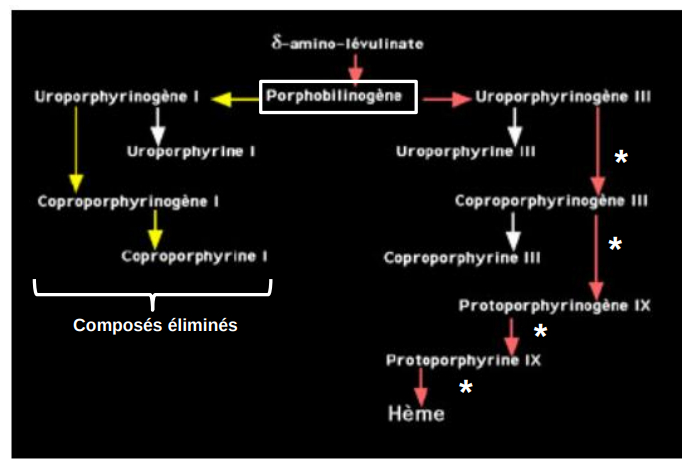
Biosynthèse des porphyrines
= voie métabolique qui conduit au noyau hème
-> comporte une voie normale = voie III - où intervient l'uropophyrinogène III cosynthétase
-> voie accessoire voie I où cette enzyme n'intervient pas et qui n'aboutit qu'à des composés éliminés dans les urines et fécès
-> enzymes qui interviennent dans la voie III :
- uroporphyrinogène I synthétase et III cosynthétase
- uroporphynogène III décarboxylase
- coproporphyrinogène oxydase
- protoporphyrinogène oxydase
- ferrochélatase
Δ-aminolévulinate ou ALA-synthétase
-> catalyse la 1ère réaction du cycle de SHZMIN
- enzyme mitochondriale d'une masse molécules de 40000 daltons
- co-enzyme : lié le phosphate de pyridoxal qui permet les réaction du carbone alpha des AA
- catalyse la condensation du glycocolle avec le succinyl-coA fournissant l'α-amino β-céto adipate
- ce produit se décarboxyle aussitôt pour aboutir au produit de la réaction enzymatique le δ-amino-lévulinate qui sort de la mitochondries
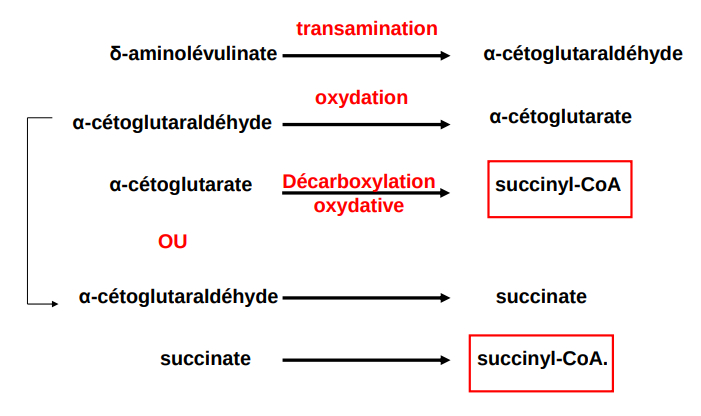
δ-aminolévulinate synthétase = inhibée allostériquement par l'hème et les hémoprotéines
-> transcription du gène est réprimée par l'hème lié à un répresseur
- mutation de ce répresseur conduit à la porphyrie intermittente aiguë
δ aminolévulinate déshydratase
= enzyme cytoplasmique qui pour cofacteurs liés l'ion Zinc et le phosphate de pyridoxal
-> catalyse la condensation de deux molécules de δ aminolévulinate pour former un cycle pyrole substituée par 3 chaînes latérales : méthylamine, acétyl, propionyl
-> produit = porphobilinogène
-> inhibée allostériquement par l'hème et les hémoprotéines
-> activité diminuée dans le saturnisme et alcoolisme
Uroporphyrinogène I synthétase
-> aussi appelée porphobilinogène cyclodésaminase ou hydroxyméthylbilane synthétase
-> catalyse la polymérisation du porphobilinogène en α-hydroxyméthylbilane
-> cyclisation se fait ensuite entre le 4ème et le 1er noyau pour former une porphyrine de la série I
-> en présence d’une uroporphyrinogène III cosynthétase le quatrième noyau pyrrol est condensé dans un sens différent des trois autres
- conduit par conséquent à un produit différent
-> intervention de la cosynthétase aboutit à un retournement du 4ème noyaux
-> perd ensuite ses radicaux acétyl, décarboxylés en méthyl
Uroporphyrinogène décarboxylase
-> enzyme commune aux voies de synthèse des porphyrines des séries I et III
-> coenzyme du cytoplasme
-> une autre décarboxylation transformera ensuite 2 des radicaux propionyl en vinyl
Coproporphyrinogène oxydase
-> enzyme mitochondriale
-> oxydation est suivie d'une bête-décarboxylation et d'une déshydratation qui produit le radical vinyl
Protoporphyrinogène oxydase
-> enzyme mitochondriale qui oxyde les carbones α, β, γ, δ et complète la désaturation du noyau tétrapyrrol
- porphyrinogène devient une porphyrine
-> productrice des radicaux libres peroxydants dont la toxicité est limitée par la présence de vit E
Ferrochélatase
= enzyme qui condense la porphyrine et l'atome de fer pour former l'hème


