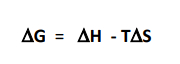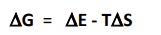= étude des variations d'énergie associées aux réactions biochimiques
-> énergie libre est l'énergie utile dans un système
- la variation de l'énergie libre selon Gibbs (deltaG) = portion de la variation totale d'énergie disponible pour accomplir une fonction au niveau cellulaire
Systèmes biologiques se conforment aux lois de la thermodynamie
-> premier principe stipule que l'énergie totale d'un système et de son milieu environnant demeure constante
- = énergie n'est ni perdue ni gagnée durant une transformation
- énergie peut être transférée d'une partie à une autre du système ou transformée en une autre forme d'énergie
-> second principe stipule que l'entropie totale d'un système doit augmenter si un processus s'effectue spontanément
- entropie représente le niveau de désordre d'un système
- relation entre la variation d'énergie libre (deltaG) d'un système en réaction et la variation de l'entropie (deltaS) est donnée par l'équation :
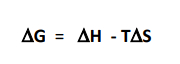
-> dans les conditions de réactions biochimiques puisque deltaH est proche de deltaE = la variation de l'énergie interne de la réaction peut s'exprimer par :
Conséquences des variations de deltaG
-> si négatif = réaction s'effectue spontanément avec perte d'énergie libre = exergonique
-> si positif = réaction ne se produit que s'il peut y avoir apport d'énergie libre = système endergonique
-> si = 0 = réaction est à l'équilibre

variation standard de l'énergie
Comment s'effectuent les réactions endergoniques
= synthèse, contraction musculaire, la conduction de l'influx nerveux et le transport actif est obtenue par couplage à des réactions d'oxydation
Nature des réactions exergoniques endergoniques
-> en pratique un processus endergonique ne peut exister d'une manière indépendante
- processus fait partie d'un système couplé exergonique-endergonique
-> réactions enzymatiques sont groupées sous le terme de catabolisme
-> réactions endergoniques = anabolisme
- processus combinés = métabolisme
Valeur de l'énergie libre des groupement phosphate de l'ATP
= généralement les gp phosphate à haute énergie sont indiqués par ~P
- ATP contient deux gp P à haute énergie = liaison phosphoanhydrire
- ADP contient un gp P " = liaison phosphoanhydride
- AMP phosphate est faiblement énergétique = liaison ester normal
ATP permet le couplage de réactions thermodynamiquement défavorbales à des réactions favorables
-> réactions endo ne peuvent pas se produire sans apport d'énergie
Interconversion des nucléotides de l’adénine et maintien de l’homéostasie énergétique (rôle de l’adénylate kinase)
-> adénylate kinase permet de maintenir l'homéostasie énergétique
-> permet :
- utilisation du phosphate à haute énergie pour la synthèse de l'ATP
- re-phosphorylation de l'AMP en ADP
- d'augmenter la concentration d'AMP quand la concentration de l'ATP diminue
Hydrolyse de l'ATP directement en AMP+ PPi
-> c'est le cas par ex lors de l'activation des acides gras à longue chaîne
D'autres nucléotides triphosphate participent au transfert des phosphates à haute énergie
-> grâce à l'enzyme nucléoside phosphate kinase, UTP, GTP et CTP peuvent être synthétisés à partir de leurs formes diphosphates
La variation d'énergie libre dans les réactions d'oxydation réduction
-> variation d'énergie libre est proportionnelle à la tendance des réactifs à donner ou à accepter des e-
- = possible d'exprimer l'énergie libre comme un potentiel d'oxydo-réduction ou potentiel rédox en volts
- enzymes impliquées dans ces processus sont appelées oxydo-réductases
- classées en 4 groupes :
- ocydases
- déshydrogénases
- hydropéroxydases
- oxygénases
Enzymes dites oxydo-réductases
Oxydases
= enzymes qui utilisent l'oxygène comme accepteur d'hydrogène
-> induisent la formation de l'eau et du peroxyde d'hydrogène
- ex : hémoprotéines, flavoprotéines qui contiennent le FAD ou FMN
Déshydrogénases
= enzymes ne peuvent pas utiliser l'oxygène comme accepteur d'hydrogène
-> fonctions principales :
- transfert d'hydrogène d'un substrat à l'autre
- transport d'e- d'un substrat à l'oxygène dans la chaîne respiratoire
Hydroperoxydases
= enzymes utilisent le peroxyde d'hydrogène ou un peroxyde organique comme substrat
-> réduisent les peroxydes en utilisant divers accepteurs d'e-
Oxygénases
= enzymes catalysent le transfert direct de l'oxygène sur un substrat
Dioxygénases
= fixent deux atomes d'une molécule d'oxygène sur un substrat
ex : L-tryptophane dioxygénase
Monooxygénases
= ou hydroxylases et oxydases à fonction mixte ne fixent qu'un seul atome d'oxygène sur un substrat
-> autre atome d'oxygène réduit en eau
ex : cytochromes P450